Чистый диоксид титана – бесцветные кристаллы, которые желтеют при нагревании, но обесцвечиваются после охлаждения. Известен в виде нескольких модификаций. Кроме рутила (кубическая сингония), анатаза (тетрагональная сингония) и брукита (ромбическая сингония), получены две модификации высокого давления: ромбическая IV и гексагональная V. Брукит при всех условиях метастабилен.
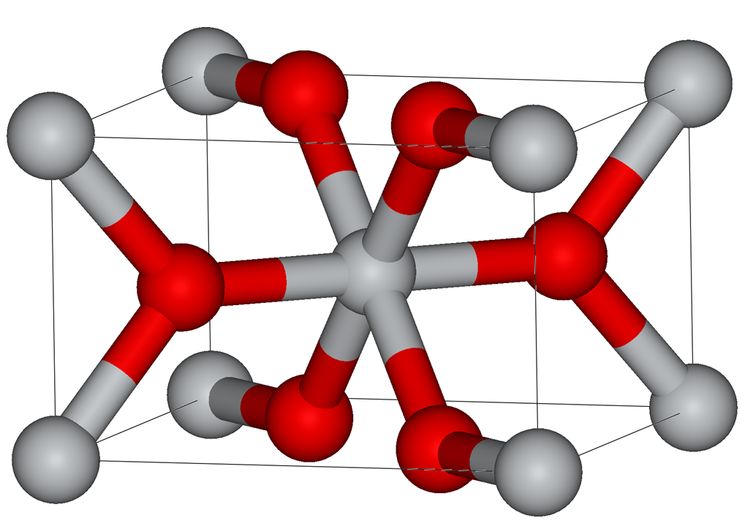
При нагревании анатаз и брукит необратимо превращаются в рутил соответственно при 400-1000°С и ~750°С. Как в рутиле, так и в анатазе каждый атом Ti находится в центре октаэдра и окружен 6 атомами кислорода. Октаэдры расположены таким образом, что каждый ион кислорода принадлежит трём октаэдрам. В анатазе на 1 октаэдр приходятся 4 общих ребра, в рутиле – 2.

Анатаз
Вследствие более плотной упаковки ионов в кристалле рутила увеличивается их взаимное притяжение, снижается фотохимическая активность, увеличиваются твёрдость (абразивность), показатель преломления (2,55 – у анатаза и 2,7 – у рутила), диэлектрическая постоянная.

Рутил
Диоксид титана не растворяется в воде и разбавленных минеральных кислотах (кроме плавиковой) и разбавленных растворах щелочей.

Ильменит
Крупные месторождения ильменита находятся в России на Южном Урале, где этот минерал был впервые открыт в Ильменских горах. Ильменит встречается во многих месторождениях Норвегии, Швеции, Украине, Финляндии, ЮАР и рудного района Садбери в Канаде, кроме того ильменитом богата лунная почва.
Медленно растворяется в концентрированной серной кислоте:
TiO2+ 2H2SO4 = Ti(SO4)2 + 2H2O
С пероксидом водорода образует ортотитановую кислоту H4TiO4:
TiO2 + 2H2O2 = H4TiO4
В концентрированных растворах щелочей:
TiO2 + 2NaOH = Na2TiO3+ H2O
При нагревании диоксид титана с аммиаком образует нитрид титана
2TiO2 + 2NH32TiN + 3H2O + O2
В насыщенном растворе гидрокарбоната калия:
TiO2 + 2KHCO3 = K2TiO3 + H2O + 2CO2
При сплавлении с оксидами, гидроксидами и карбонатами образуются титанаты и двойные оксиды:
TiO2 + BaO = BaOxTiO2(BaTiO3)
TiO2 + BaCO3 = BaOxTiO2 + CO2(BaTiO3)
TiO2 + Ba(OH)2 = BaOxTiO2(BaTiO3)

Водородом, углеродом и активными металлами (Mg, Ca, Na) диоксид титана при нагревании восстанавливается до низших оксидов, а с хлором при нагревании в присутствии восстановителей (углерода) образует тетрахлорид титана.

Гидроксид TiO2xnH2O в зависимости от условий его осаждения может содержать переменное число связанных с титаном ОН-групп. Полученный при невысоких температурах TiO2xnH2O (?-форма) хорошо растворяется в разбавленных минеральных и сильных органических кислотах, но практически не растворяется в растворах щелочей, легко пептизируется с образованием устойчивых коллоидных растворов.
После сушки на воздухе образует белый порошок плотностью 2,6 г/см3, приближающийся по составу к формуле TiO2x2H2O (метатитановая кислота).











